비엘팜텍은 시가총액 수조원에 달하는 기업들과 분자접착제 기술 이전을 논의하고 있다는 내용이 담긴 팜이데일리 유료 기사가 영향을 미친 것으로 보인다. 앱클론은 전환우선주 전량이 보통주로 전환돼 오버행(잠재적 매도물량) 불확실성 완전 해소됐다는 점이 주가에 긍정적으로 작용했다. 현대바이오사이언스는 호흡기 바이러스 질환 바스켓 임상 2상 미국 식품의약국(FDA) 신청 결정이 이틀째 주가를 끌어올렸다.

15일 비엘팜텍 추가 추이. (이미지=엠피닥터)
◇ 비엘팜텍, 분자접착제 플랫폼 기술 이전 논의
이날 KG제로인 엠피닥터(MP DOCTOR·옛 마켓포인트)에 따르면 비엘팜텍의 주가는 전일대비 29.86% 급등한 635원을 기록했다. 팜이데일리 '시총 6·11·26조 기업들과 동시 협상'… 비엘팜텍, 분자접착제로 조 단위 빅딜 정조준 기사에 따르면 비엘팜텍은 시가총액 수조원에 달하는 기업들과 분자접착제 플랫폼 기술 이전 논의를 진행하고 있는 것으로 알려졌다.
비알팜텍의 자회사 비엘멜라니스는 분자접착제 기반의 표적 단백질 분해(TPD) 항암제를 개발하고 있다. 비엘멜라니스가 개발하는 항암제는 전체 암의 약 10%를 차지하는 대안적 텔로머라아제 유지 기전(ALT) 암과 기존 치료제에 내성을 보이는 림프종을 표적으로 한다.
분자접착제는 암 관련 표적 단백질을 E3 유비퀴틴 리가제와 강제로 결합시켜 프로테아좀에서 완전히 분해시킨다. 분자접착제는 기존 키나아제 억제제 대비 내성 발생 가능성이 적다.
앞서 비엘멜라니스의 분자접착제는 지난해 11월 다국적 제약사인 암젠(Amgen)이 주최하는 '2025 골든티켓' 프로그램에서 최종 수상자로 이름을 올렸다. 당시 40여 개 기업이 참여했다.
이 중 수상기업은 인공지능(AI) 분석으로 약물을 발굴하는 포트레이와 비엘멜라니스 둘 뿐이었다. 신약 개발사로 한정하면 비엘멜라니스 뿐이었다. 비엘팜텍은 비엘멜라니스의 지분 34.91%를 보유하고 있다.
이번 수상으로 비엘멜라니스는 △암젠 글로벌 연구개발(R&D) 전문가 멘토링 △보건산업혁신창업센터 내 암젠 골든티켓 센터 입주 △임상 설계 등 글로벌 컨설팅 지원 등을 제공받게 된다. 암젠 골든티켓 프로그램은 한국이 △미국 △캐나다 △싱가포르 △프랑스에 이어 전 세계에서 다섯 번째로 도입한 국가로 전해진다.
글로벌 시장조사기관 그랜드뷰리서치(Grand View Research)는 분자접착제 기반 항암제 시장이 2024년 5억4000만달러(약 8000억원)에서 2030년 16억9000만달러(약 2조5000억원)로 연평균 20.8% 성장할 것으로 전망했다.
비엘멜라니스 관계자는 “기술 비공개 기조를 유지해 왔으나 암젠 수상을 계기로 글로벌 빅파마와 공동 연구개발·기술협력 논의를 본격화할 계획”이라며 “관심 있는 국내외 투자자를 대상으로 기업설명회(IR)도 확대할 것”이라고 말했다.
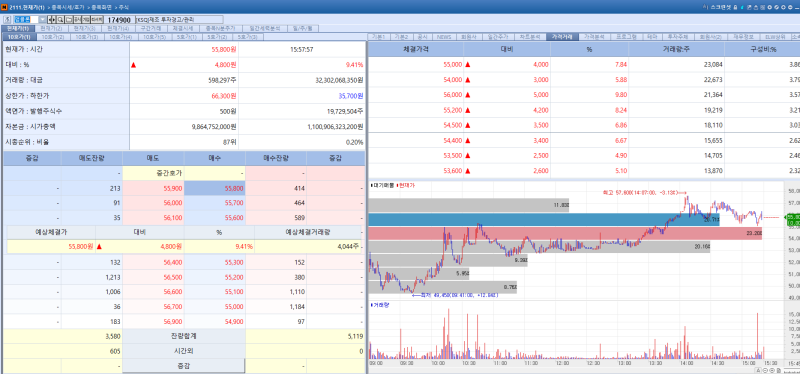
15일 앱클론 주가 추이. (이미지=엠피닥터)
◇ 앱클론, 전환우선주 보총주 전환 청구 완료료 오버행 우려 해소
항체 신약개발 전문기업 앱클론의 이날 주가는 전일대비 9.41% 오른 5만5800원을 나타냈다. 앱클론은 오버행 우려가 해소된 점이 주가를 끌어올렸다. 앱클론은 기발행된 전환우선주(CPS)의 보통주 전환 청구가 완료돼 금일 대부분의 물량인 61만7163주가 상장되고 내주에 잔량 전부가 상장됐다고 밝혔다. 이를 통해 잠재적 대기 물량의 불확실성을 완전히 해소했다.
앱클론은 이번 자본 구조 단순화가 글로벌 파트너사 헨리우스의 임상 성과 발표와 맞물려 기업가치 재평가의 원년이 될 것으로 전망했다. 앱클론의 기술이 적용된 위암 치료제 AC101(현지명 HLX22)이 미국임상종양학회 소화기암 심포지엄(ASCO GI 2026)에서 기존 치료제의 한계를 뛰어넘는 데이터를 공개하며 시장의 이목을 집중시켰다.
헨리우스가 발표한 임상 2상(HLX22-GC-201) 장기 추적 결과에 따르면 HER2 양성 위암 환자 1차 치료에서 HLX22 병용 투여군은 무진행 생존기간 중앙값(mPFS)이 데이터 분석 시점까지 도달하지 않은 반면 대조군(표준요법)은 8.3개월에 그쳤다
주목할 점은 위험비(HR)가 0.20(95% 신뢰구간 0.09-0.54)을 기록해 대조군 대비 질병 진행 위험을 80% 낮추는 효능을 입증했다는 것이다. 항암제 임상에서 0.7~0.8을 기록해도 성공이라 평가하기에 0.2를 기록한 것은 매우 고무적인 수치라는 것이 앱클론의 설명이다.
투여 24개월 시점의 무진행 생존율(PFS rate)은 HLX22 병용군이 54.8%로, 대조군(17.5%) 대비 3배 이상 높은 생존율을 보였다. 이는 기존 경쟁 약물들의 임상 결과인 펨브롤리주맙 병용요법(10.0개월), 퍼투주맙 병용요법(8.5개월) 등을 크게 웃돈다.
헨리우스는 이번 학회에서 긍정적인 임상 2상 결과를 바탕으로 진행 중인 글로벌 임상 3상(HLX22-GC-301) 계획도 함께 발표했다. 임상 3상은 전 세계 550명의 환자를 대상으로 진행된다. 임상 3상ㄹ은 면역항암제 혜택을 보기 어려운 PD-L1 저발현 환자군까지 포괄해 시장성을 극대화할 예정이다.
앱클론 관계자는 “이번 보통주 전환은 자본 내 구성 항목을 정리해 자본 구조를 단순화하고 오버행에 대한 불확실성을 해소했다는 데 의미가 있다”며 “이와 동시에 AC101의 HR 0.20라는 데이터를 확인하게 돼 기쁘게 생각한다. 숫자가 증명하는 기업의 본질 가치를 시장에 알릴 수 있게 됐다”고 말했다.
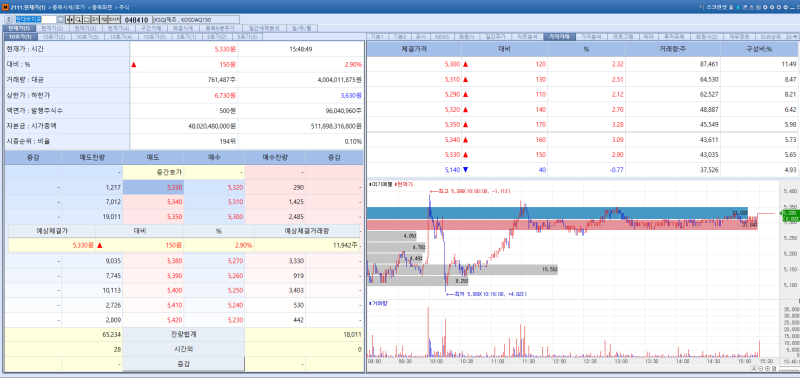
현대바이오사이언스 15일 주가 추이. (이미지=엠피닥터)
◇ 현대바이오, 호흡기 바이러스 질환 바스켓 2상 FDA 신청 결정
현대바이오의 주가는 전일대비 2.90% 상승한 5330원을 기록했다. 현대바이오의 주가는 전일에 이어 이틀째 상승했다. 현대바이오가 인플루엔자 등 여러 호흡기 바이러스 질환을 대상으로 하는 바스켓 임상 2상을 FDA에 신청하기로 확정한 점이 호재로 작용했다.
현대바이오는 최근 미국 샌프란시스코에서 열린 '2026 바이오텍 쇼케이스'에서 미국 보건당국 전문가들과 글로벌 대감염해결 전략을 심도 있게 논의한 결과를 바탕으로 이같이 결정했다. 현대바이오는 FDA와의 임상시험계획(IND) 실무를 전담할 현지 임상수탁기관(CRO) 선정을 마무리했다.
임상 총괄 책임을 맡게 된 데이비드 스미스 캘리포니아대 샌디에이고(UCSD) 교수는 미국 정부의 코로나19 국책 임상(ACTIV-2)에서 국제 프로토콜 의장으로서 치료제 선정과 임상 전반을 지휘했던 세계적인 감염병 석학으로 전해진다.
현대바이오 관계자는 "바이오텍 쇼케이스 이전부터 미국 보건당국 전문가들과 전략적 논의를 이어오며 미국 임상 2상 준비를 구체화해 왔다"며 "닥터 스미스 교수를 임상 총괄 책임자로 선임하고 현지 CRO와 계약까지 마친 만큼 본격적인 임상 신청을 위한 FDA 절차를 지체 없이 진행하겠다"고 말했다.